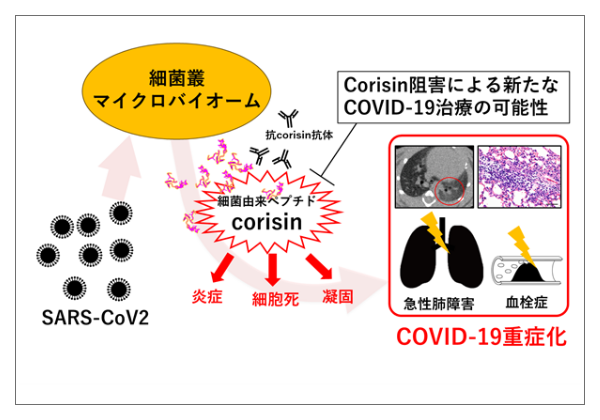
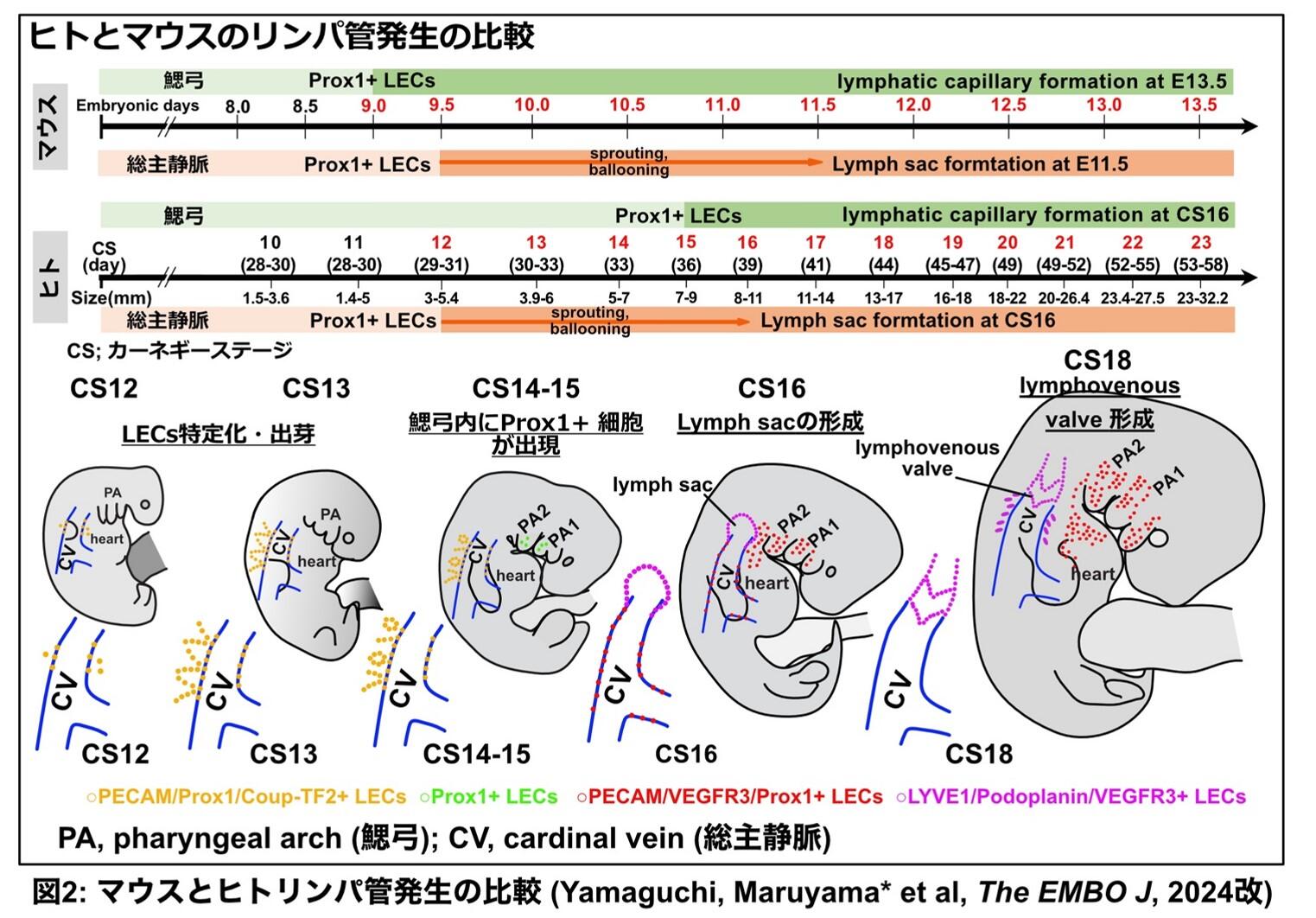
病理学は、疾患とその基盤となる組織・細胞・分子レベルでの変化を統合する学術分野で、基礎科学と臨床医学の架け橋です。病変が生じた組織では、細胞の種類と配置が変わり組織の構造が変化します。この現象は組織リモデリングと呼ばれ、細胞死、炎症、再生や癌などの病変で普遍的に見られます。私たちの研究分野では、この現象に伴って一過性に高発現する細胞外マトリックス分子であるテネイシン-Cを中心に、組織リモデリングのメカニズムを研究しています。この分子をマーカーとする病気の組織診断や体内・体外診断の方法の開発をはじめとし、組織リモデリングの抑制・促進を制御することによる治療法を追い求めています。
- 教 授
- 今中恭子
(三重大学マトリックスバイオロジー研究センター長) - 学内講師
- 橋詰令太郎
- 学部担当科目
- 病理学
- 附属病院診療科
- 病理部/病理診断科
- 居室
- 探索医学研究棟 3階
研究・教育内容
さまざまな原因からおこるいろいろな病気は一見違った現象にみえますが、基本的には同じような進行の仕方をします。つまり、臓器などに炎症が生じると、組織では細胞と細胞外マトリックスの構成に変化が起こり、組織リモデリングが生じます。この時に過度の変化が生じると、線維化が起き臓器の機能が失われることがあります。具体的には肝硬変や肺線維症などであり、この状態から治療することはかなり困難となります。当研究室が研究を続けている分子テネイシン-C(TNC)は、この過程の組織リモデリングの最盛期に特徴的に出現する細胞外マトリックスタンパクです。TNCは組織リモデリングの方向性と進行速度を決定づけると考え、さまざまな疾患での役割を研究してきました。また、発生期における役割についても、心臓を中心として研究を行っています。
TNCを標的として検査をすれば、病気の部位や病気の進行の速さを診断でき、臓器の機能がなくなる前に治療を効果的に行えます。心筋梗塞などの心疾患の診断、老人に多い変形性骨関節症の進行度、慢性肝炎の活動度、くも膜下出血後の合併症の予測や乳癌など癌の進行度の評価にも有用であることを発表してきました。また、この分子を治療標的とすれば、組織再構築の制御が可能で、たとえば抑制することにより、心臓血管のバイパス術後の血管閉塞などが予防できます。逆に促進効果を利用し、くも膜下出血の原因である動脈瘤の血管内治療や関節軟骨の再生を目指しています。これらの研究は、「三重大学マトリックスバイオロジー研究センター」のメンバーと共同で行っています。
また、腫瘍や染色体疾患の多くは、染色体の数的増加を伴います。核型正常化による細胞再生の可能性も探究しています(図4,5)。
大学院入学後病理診断の研修を平行して行うことにより、病理専門医を取得することができます。また、研究してみたい学部学生を歓迎します。一流雑誌に論文を発表した先輩もいます。





研究業績
-
Serum Tenascin-C as a Novel Predictor for Risk of Coronary Artery Lesion and Resistance to Intravenous Immunoglobulin in Kawasaki Disease - A Multicenter Retrospective Study.
Okuma Y, Suda K, Nakaoka H, Katsube Y, Mitani Y, Yoshikane Y, Ichida F, Matsushita T, Shichino H, Shiraishi I, Abe J, Hiroe M, Yoshida T, Imanaka-Yoshida K.
Circ J. 2016 Oct 25;80(11):2376-2381. -
Tenascin-C may accelerate cardiac fibrosis by activating macrophages via the integrin αVβ3/nuclear factor-κB/interleukin-6 axis.
Shimojo N, Hashizume R, Kanayama K, Hara M, Suzuki Y, Nishioka T, Hiroe M, Yoshida T, Imanaka-Yoshida K.
Hypertension. 2015 Oct;66(4):757-66. -
Binding of αvβ1 and αvβ6 integrins to tenascin-C induces epithelial-mesenchymal transition-like change of breast cancer cells.
Katoh D, Nagaharu K, Shimojo N, Hanamura N, Yamashita M, Kozuka Y, Imanaka-Yoshida K, Yoshida T.
Oncogenesis. 2013 Aug 19;2:e65.. -
Tenascin C induces epithelial-mesenchymal transition-like change accompanied by SRC activation and focal adhesion kinase phosphorylation in human breast cancer cells.
Nagaharu K, Zhang X, Yoshida T, Katoh D, Hanamura N, Kozuka Y, Ogawa T, Shiraishi T, Imanaka-Yoshida K.
Am J Pathol. 2011 Feb;178(2):754-63.. -
Tenascin-C may aggravate left ventricular remodeling and function after myocardial infarction in mice.
Nishioka T, Onishi K, Shimojo N, Nagano Y, Matsusaka H, Ikeuchi M, Ide T, Tsutsui H, Hiroe M, Yoshida T, Imanaka-Yoshida K.
Am J Physiol Heart Circ Physiol. 2010 Mar;298(3):H1072-8. -
Role of stromal tenascin-C in mouse prostatic development and epithelial cell differentiation.
Ishii K, Imanaka-Yoshida K, Yoshida T, Sugimura Y.
Dev Biol. 2008 Dec 15;324(2):310-9. Epub 2008 Oct 10. -
Deficiency of tenascin-C attenuates liver fibrosis in immune-mediated chronic hepatitis in mice.
El-Karef A, Yoshida T, Gabazza EC, Nishioka T, Inada H, Sakakura T, Imanaka-Yoshida K.
J Pathol. 2007 Jan;211(1):86-94. -
Serum tenascin-C might be a novel predictor of left ventricular remodeling and prognosis after acute myocardial infarction.
Sato A, Aonuma K, Imanaka-Yoshida K, Yoshida T, Isobe M, Kawase D, Kinoshita N, Yazaki Y, Hiroe M.
J Am Coll Cardiol. 2006 Jun 6;47(11):2319-25. -
Tenascin-C regulates recruitment of myofibroblasts during tissue repair after myocardial injury.
Tamaoki M, Imanaka-Yoshida K, Yokoyama K, Nishioka T, Inada H, Hiroe M, Sakakura T, Yoshida T.
Am J Pathol. 2005 Jul;167(1):71-80. -
Involvement of large tenascin-C splice variants in breast cancer progression.
Tsunoda T, Inada H, Kalembeyi I, Imanaka-Yoshida K, Sakakibara M, Okada R, Katsuta K, Sakakura T, Majima Y, Yoshida T.
Am J Pathol. 2003 Jun;162(6):1857-67.